
Saturs
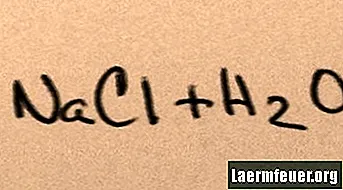
Pievienojot sāli ūdenim, tas izšķīst tā sastāvdaļu molekulās, līdz ap ūdeņraža un skābekļa molekulām peld maksimālie sāls joni, kurus ūdens var uzturēt. Kad tas notiek, šķīdumu sauc par "piesātinātu". Kad izšķīdis vairāk sāls, nātrija un hlorīda joni saduras viens ar otru un rekombinējas sāls kristālos. Šī parādība ir pazīstama kā "nokrišņi", jo izveidojusies cieta viela nokrīt ūdens dibenā. Sāļi ir "hidrofīli", tas ir, tos piesaista ūdens. Šī pievilcība atvieglo pazīstamu nokrišņu formu: lietus lāses veidojas ap sīkiem sāls kristāliem mākoņos, padarot to nedaudz sāļu.
Pamata

Elektrolīti

Sāls nepadara elektrību cietā stāvoklī, bet šķidrā (šķidrā) stāvoklī tas veido risinājumu, kas ļoti labi var vadīt elektrību. Vadītspēja ir atkarīga no izmantotā sāls veida, taču šie šķidrumi, ko sauc par elektrolītu šķīdumiem, ir lieliski savienojumi, kas nepieciešami cilvēka ķermenim. Smadzeņu radītie elektriskie impulsi rada brīvu skābekli, ko lieto asinis. Sāls molekulas tiek klasificētas elektrolītos (nātrijā, kālijā vai kalcijā) un hlorīdos šķīdumā: hlorīdu asinis un nieres pumpē urīnā, un elektrolīti tiek izplatīti caur neiromuskulāro sistēmu procesā, ko sportisti sauc rehidratācija.
Koligatīvās īpašības

Jebkurš šķīdums atšķiras no tā sākotnējā sastāva, jo molekulu pievienošana, pat ja tās neveido jaunus savienojumus, maina šķidruma molekulmasu un ietekmē tā īpašības. Sālsūdens ir blīvāks par tīru ūdeni un sasalst arī lēnāk. Sasalstot, sāls tomēr migrē līdz šķidruma robežām, padarot to smagāku un piesātinātāku, un pēc tam pazemina sasalšanas temperatūru. Vielas stāvokļa otrajā galā, jo blīvāks ir sāļais ūdens, jo vairāk siltuma tam nepieciešams iztvaikot, līdz ūdens iztek, atstājot sāls slāni. Pavāri gaida, līdz katlā vārās ūdens, lai pievienotu sāli, lai nekavētu karsēšanu. Šīs īpašības, kas pazīstamas kā "koligatīvās īpašības", palīdz zinātniekiem noteikt sālsūdens molekulmasu. Ja var izmērīt šķidruma masu, atmosfēras spiedienu un viršanas temperatūru, tad zinātnieki var atņemt ūdens molekulmasu, lai uzzinātu, kuri sāļi ir klāt.